在容积不变的密闭容器中有反应:X(g) + Y(g) 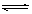 z(g),若Z(g)的物质的量浓度c(Z)
z(g),若Z(g)的物质的量浓度c(Z) 与温度T的关系如右图所示。
与温度T的关系如右图所示。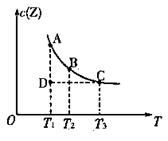
则下列说法不正确的是
A.A点与B点相比,B点的c (X)大
B.A点与C点的化学反应速率:前者<后者
C.在反应进行到D点时,V正<V逆
D.A、B、C点都表示该反应达平衡状态
在容积不变的密闭容器中有反应:X(g) + Y(g) 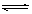 z(g),若Z(g)的物质的量浓度c(Z)
z(g),若Z(g)的物质的量浓度c(Z) 与温度T的关系如右图所示。
与温度T的关系如右图所示。
则下列说法不正确的是
A.A点与B点相比,B点的c (X)大
B.A点与C点的化学反应速率:前者<后者
C.在反应进行到D点时,V正<V逆
D.A、B、C点都表示该反应达平衡状态