按要求回答下列问题:
(1)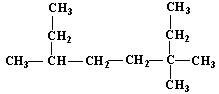 的名称为___________________________;
的名称为___________________________;
(2)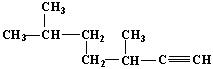 的名称为____________________________;
的名称为____________________________;
(3)2,4-二氯甲苯的结构简式为_________________________ ___;
___;
(4)某物质结构如图所示,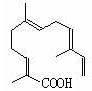
碳原子数为 ;
该物质可以与下列 (填序号)发生反应。
| A.KMnO4酸性溶液 | B.氢气 | C.溴水 | D.NaOH溶液 |
按要求回答下列问题:
(1)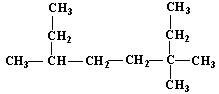 的名称为___________________________;
的名称为___________________________;
(2) 的名称为____________________________;
的名称为____________________________;
(3)2,4-二氯甲苯的结构简式为_________________________ ___;
___;
(4)某物质结构如图所示,
碳原子数为 ;
该物质可以与下列 (填序号)发生反应。
| A.KMnO4酸性溶液 | B.氢气 | C.溴水 | D.NaOH溶液 |