实验室利用右图装置进行中和热的测定,请回答下列问题: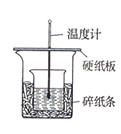
(1)在操作正确的前提下,提高中和热测定准确性的关键是
(2)做1次完整的中和热测定实验,温度计需使用 次,
某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别
测量酸和碱的温度,你是否同意该同学的观点,为什么?
(3)请为本实验设计数据记录表格:
实验室利用右图装置进行中和热的测定,请回答下列问题:
(1)在操作正确的前提下,提高中和热测定准确性的关键是
(2)做1次完整的中和热测定实验,温度计需使用 次,
某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别
测量酸和碱的温度,你是否同意该同学的观点,为什么?
(3)请为本实验设计数据记录表格: