可逆反应:2NO2(g)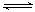 2NO(g) + O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
2NO(g) + O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2 n mol NO2 ②单位时间内生成n mol O2的同时生成2 n mol NO ③用NO2、NO、O2表示的反应速率数值之比为2∶2∶1的状态 ④混合气体的颜色不再改变的状态
| A.①④ | B.②③ | C.①③④ | D.①②③④ |
可逆反应:2NO2(g)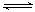 2NO(g) + O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
2NO(g) + O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2 n mol NO2 ②单位时间内生成n mol O2的同时生成2 n mol NO ③用NO2、NO、O2表示的反应速率数值之比为2∶2∶1的状态 ④混合气体的颜色不再改变的状态
| A.①④ | B.②③ | C.①③④ | D.①②③④ |