(4分)下面列出了几组物质,请将物质的合适组号填写在空格上。互为同位素的是 ,互为同分异构体的是 ,互为同系物的是 ,互为同素异形体的是 。
①金刚石与“足球烯”C60; ②D2O与T2O; ③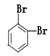 和
和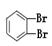
④CH4和CH3CH2CH3; ⑤葡萄糖与果糖; ⑥16O和18O
(4分)下面列出了几组物质,请将物质的合适组号填写在空格上。互为同位素的是 ,互为同分异构体的是 ,互为同系物的是 ,互为同素异形体的是 。
①金刚石与“足球烯”C60; ②D2O与T2O; ③ 和
和
④CH4和CH3CH2CH3; ⑤葡萄糖与果糖; ⑥16O和18O