缩聚产物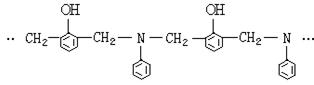 是一种具有较好耐热性、耐水性和高频电绝缘性的高分子化合物(树脂),它是由三种单体在一定条件下缩聚(同时还生成水)而成的。这三种单体分别是(写结构简式)C6H5NH2、 和 。
是一种具有较好耐热性、耐水性和高频电绝缘性的高分子化合物(树脂),它是由三种单体在一定条件下缩聚(同时还生成水)而成的。这三种单体分别是(写结构简式)C6H5NH2、 和 。
它们的物质的量之比(按以上回答单体的顺序写)为 。
缩聚产物 是一种具有较好耐热性、耐水性和高频电绝缘性的高分子化合物(树脂),它是由三种单体在一定条件下缩聚(同时还生成水)而成的。这三种单体分别是(写结构简式)C6H5NH2、 和 。
是一种具有较好耐热性、耐水性和高频电绝缘性的高分子化合物(树脂),它是由三种单体在一定条件下缩聚(同时还生成水)而成的。这三种单体分别是(写结构简式)C6H5NH2、 和 。
它们的物质的量之比(按以上回答单体的顺序写)为 。