2002年诺贝尔化学奖获得者的贡献之一是发明了对有机物分子进行结构分析的质谱法。其方法是让极少量的(10-9g)化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+,然后测定其质荷比。某有机物样品的质荷比如图所示。该有机物可能是
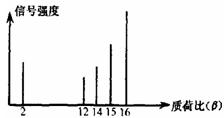
| A.甲醇 | B.甲烷 | C.丙烷 | D.乙烯 |
2002年诺贝尔化学奖获得者的贡献之一是发明了对有机物分子进行结构分析的质谱法。其方法是让极少量的(10-9g)化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+,然后测定其质荷比。某有机物样品的质荷比如图所示。该有机物可能是

| A.甲醇 | B.甲烷 | C.丙烷 | D.乙烯 |