某有机化合物A的相对分子质量(分子量)大于110,小于 150。经分析得知,其中碳和氢的质量分数之和为52.24%,其
150。经分析得知,其中碳和氢的质量分数之和为52.24%,其 余为氧。请回答:
余为氧。请回答:
(1)该化合物分子中含有几个氧原子?为什么?
(2)该化合物的相对分子质量是 。
(3)该化合物的化学 式是 。
式是 。
(4)该化合物分子中最多含 个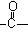 官能团。
官能团。
某有机化合物A的相对分子质量(分子量)大于110,小于 150。经分析得知,其中碳和氢的质量分数之和为52.24%,其
150。经分析得知,其中碳和氢的质量分数之和为52.24%,其 余为氧。请回答:
余为氧。请回答:
(1)该化合物分子中含有几个氧原子?为什么?
(2)该化合物的相对分子质量是 。
(3)该化合物的化学 式是 。
式是 。
(4)该化合物分子中最多含 个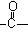 官能团。
官能团。