实验室用下图装置制取少量溴苯,试填写下列空白。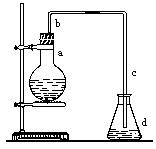
(1)在烧瓶a中装的试剂是 、 、 。
(2)请你推测长直导管b的作用是 。
(3)请你推测导管c的下口可否浸没于液面中
(4)写出烧瓶a中所有反应的方程式(标明条件)并指出有机反应类型________。
实验室用下图装置制取少量溴苯,试填写下列空白。
(1)在烧瓶a中装的试剂是 、 、 。
(2)请你推测长直导管b的作用是 。
(3)请你推测导管c的下口可否浸没于液面中
(4)写出烧瓶a中所有反应的方程式(标明条件)并指出有机反应类型________。