下列五组物质中___互为同位素, ___ 是同分异构体,___ 是同系物。
① 
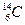 ②白磷 红磷 ③
②白磷 红磷 ③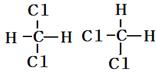
④CH3CH3 CH3CH(CH3)CH3 ⑤CH3CH(CH3)CH2CH3 C(CH3)4
下列五组物质中___互为同位素, ___ 是同分异构体,___ 是同系物。
① 
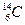 ②白磷 红磷 ③
②白磷 红磷 ③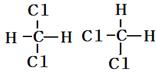
④CH3CH3 CH3CH(CH3)CH3 ⑤CH3CH(CH3)CH2CH3 C(CH3)4