中性物质 A可发生下列变化,且B、D、E均可发生银镜反应,G的核磁共振氢谱中只有一个吸收峰。
A可发生下列变化,且B、D、E均可发生银镜反应,G的核磁共振氢谱中只有一个吸收峰。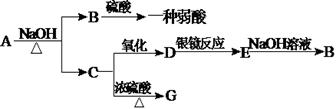
(1)  推断下述物质的结构简式:
推断下述物质的结构简式:
A:________________ D: ________________
(2)写出下列变化的化学方程式:
A+NaOH→B+C:_____________________________________________
C→G:________________________________________________
中性物质 A可发生下列变化,且B、D、E均可发生银镜反应,G的核磁共振氢谱中只有一个吸收峰。
A可发生下列变化,且B、D、E均可发生银镜反应,G的核磁共振氢谱中只有一个吸收峰。
(1)  推断下述物质的结构简式:
推断下述物质的结构简式:
A:________________ D: ________________
(2)写出下列变化的化学方程式:
A+NaOH→B+C:_____________________________________________
C→G:________________________________________________