某储能电池的原理如图所示,溶液中c(H+) =" 2.0" mol·L-1,阴离子为SO42-,a、b均为惰性电极,充电过程中左槽溶液颜色由蓝色变为黄色。下列叙述正确的是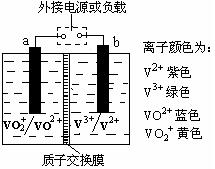
| A.当右槽溶液颜色由绿色变为紫色时,电池中能量转化形式为化学能转化为电能 |
| B.充电过程中,a极的反应式为VO2+-e-+ H2O = VO2++ 2H+ |
| C.储能电池a、b两极间的电解质溶液中通过电子的定向移动形成闭合回路 |
| D.放电时, H+从左槽迁移进入右槽 |
某储能电池的原理如图所示,溶液中c(H+) =" 2.0" mol·L-1,阴离子为SO42-,a、b均为惰性电极,充电过程中左槽溶液颜色由蓝色变为黄色。下列叙述正确的是
| A.当右槽溶液颜色由绿色变为紫色时,电池中能量转化形式为化学能转化为电能 |
| B.充电过程中,a极的反应式为VO2+-e-+ H2O = VO2++ 2H+ |
| C.储能电池a、b两极间的电解质溶液中通过电子的定向移动形成闭合回路 |
| D.放电时, H+从左槽迁移进入右槽 |