(12分)下图是一个制取氯气并以氯气为原料进行某些反应的装置。(夹持和加热装置省略)。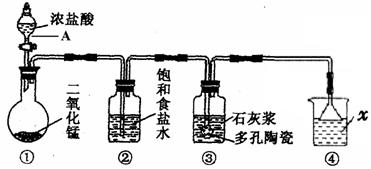
(1)写出图中仪器A的名称: 。
(2)装置中x试剂为 ;装置中饱和食盐水的作用是 。
(3)装置③中发生反应的化学方程式为 。
(4)若将生成的C12通入淀粉碘化钾无色溶液中,可观察到溶液变成 色,反应的离子方程式为 。
(12分)下图是一个制取氯气并以氯气为原料进行某些反应的装置。(夹持和加热装置省略)。
(1)写出图中仪器A的名称: 。
(2)装置中x试剂为 ;装置中饱和食盐水的作用是 。
(3)装置③中发生反应的化学方程式为 。
(4)若将生成的C12通入淀粉碘化钾无色溶液中,可观察到溶液变成 色,反应的离子方程式为 。