氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O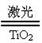 2H2↑+O2↑ 。制得的氢气可用于燃料电池。试完成下列问题:
2H2↑+O2↑ 。制得的氢气可用于燃料电池。试完成下列问题:
太阳光分解海水时,实现了从_______能转化为_______能,二氧化钛作________。生成的氢气,用于燃料电池时,实现________能转化为________能。燃料电池中通入氢气的是 极(填“正”或“负”),分解海水的反应属于________反应(填“放热”或“吸热”)。
氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O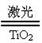 2H2↑+O2↑ 。制得的氢气可用于燃料电池。试完成下列问题:
2H2↑+O2↑ 。制得的氢气可用于燃料电池。试完成下列问题:
太阳光分解海水时,实现了从_______能转化为_______能,二氧化钛作________。生成的氢气,用于燃料电池时,实现________能转化为________能。燃料电池中通入氢气的是 极(填“正”或“负”),分解海水的反应属于________反应(填“放热”或“吸热”)。