在体积固定为2 L的密闭容器中,A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化情况如图甲所示。下列有关说法不正确的是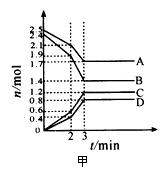
A.该反应的化学方程式为4A + 5B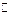 6C + 4D
6C + 4D
B.前2 min用B表示的反应速率约为0.0021 mol·L-1·s-1
C.2 min时,外界条件的改变可能是升高温度或加入了催化剂
D.若起始时只加入A、B且物质的量分别为1.6 mol和2.0 mol,则达平衡时A、B的转化率不相等
在体积固定为2 L的密闭容器中,A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化情况如图甲所示。下列有关说法不正确的是
A.该反应的化学方程式为4A + 5B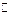 6C + 4D
6C + 4D
B.前2 min用B表示的反应速率约为0.0021 mol·L-1·s-1
C.2 min时,外界条件的改变可能是升高温度或加入了催化剂
D.若起始时只加入A、B且物质的量分别为1.6 mol和2.0 mol,则达平衡时A、B的转化率不相等