下图中的每一个方格表示有关的一种反应物或生成物,其中A,C,D为无色气体.请填下列空白: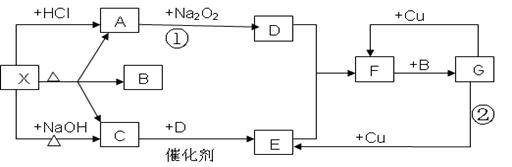
(1)物质X可以是______________________,C 是____________,F是____________.
(2)反应①化学方程式是________________________________________________。
(3)反应②的离子方程式是______________________________________________。
下图中的每一个方格表示有关的一种反应物或生成物,其中A,C,D为无色气体.请填下列空白:
(1)物质X可以是______________________,C 是____________,F是____________.
(2)反应①化学方程式是________________________________________________。
(3)反应②的离子方程式是______________________________________________。