从某A的水溶液出发,有下图一系列变化(参加反应的水和生成的水均没有表示),已知D的焰色反应为紫色。
⑴写出化学式:A ▲ E ▲ Y ▲
⑵写出①、②反应离子方程式 ▲ , ▲
⑶Y有毒,含Y水溶液可加W检验其存在。还可向其水溶液中滴加 ▲ 检验其存在,该反应的化学方程式为: ▲ 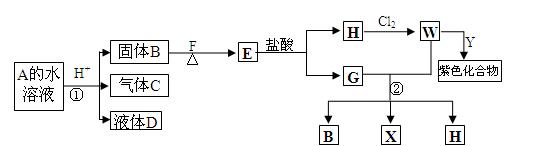
从某A的水溶液出发,有下图一系列变化(参加反应的水和生成的水均没有表示),已知D的焰色反应为紫色。
⑴写出化学式:A ▲ E ▲ Y ▲
⑵写出①、②反应离子方程式 ▲ , ▲
⑶Y有毒,含Y水溶液可加W检验其存在。还可向其水溶液中滴加 ▲ 检验其存在,该反应的化学方程式为: ▲ 