Ⅰ)⑴已知:N2(g)+O2(g)=2NO(g);△H=+180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905kJ·mol-1
2H2(g)十O2(g)=2H2O(g):△H=-483.6kJ·mol-1
则N2(g)+3H2(g) 2NH3(g)的△H= ▲ 。
2NH3(g)的△H= ▲ 。
⑵在一定条件下,将2molN2与5molH2混合于一个10L的密闭容器中,反应情况如图1所示:
①求5min内的平均反应速率v(NH3) ▲ ;
②达到平衡时NH3的体积分数为 ▲ 。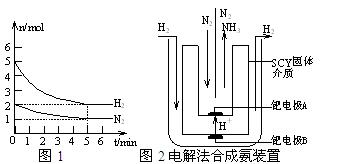
⑶近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图2)。钯电极A上发生的电极反应式是 ▲ 。
Ⅱ)甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
①CH4(g)+H2O(g)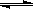 CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1
②CO(g)+2H2(g)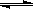 CH3OH(g) ΔH2
CH3OH(g) ΔH2
将0.20molCH4和0.30molH2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如右图。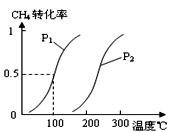
(1)温度不变,缩小体积,增大压强,①的反应速率 ▲ (填“增大”、“减小”或“不变”),平衡向 ▲ 方向移动。
(2)反应①的△H1 ▲ 0(填“<”、“=”或“>”)。
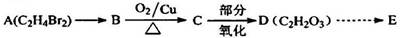
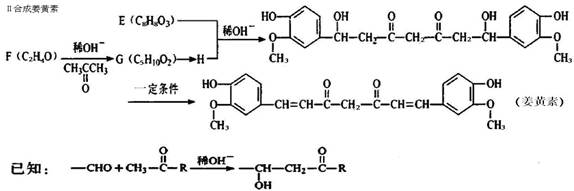

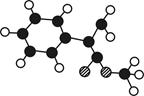
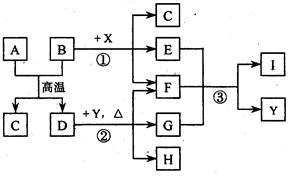
 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下:
 粤公网安备 44130202000953号
粤公网安备 44130202000953号