将一定质量的Mg,Al合金全部溶解在500mL盐酸中(体积变化不计),取10mL反应后的溶液,用1mol/LNaOH溶液滴定得下图关系。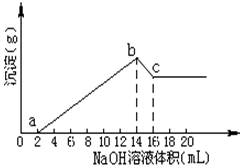
(1)原合金中Mg的质量为 g;Al的质量为 g
(2)盐酸的物质的量浓度为 mol/L
将一定质量的Mg,Al合金全部溶解在500mL盐酸中(体积变化不计),取10mL反应后的溶液,用1mol/LNaOH溶液滴定得下图关系。
(1)原合金中Mg的质量为 g;Al的质量为 g
(2)盐酸的物质的量浓度为 mol/L