一定条件下,体积为2L的密闭容器中,1mol A和1mo1 B进行反应:A(g)+3B(g) 2C(g) 经2分钟反应达到平衡,此时生成0.2mol C。
2C(g) 经2分钟反应达到平衡,此时生成0.2mol C。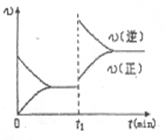
下列说法正确的是
A.反应开始至2分钟时,以B浓度变化表示的反应速率为0.05mol/(L.min)
B.反应开始至2分钟时,A的转化率为5%
C.若其他条件不变,升高温度,A的体积分数增大,则该反应的△H<0
D.若其他条件不变,增大压强,化学反应速率的变化符合右侧示意图
一定条件下,体积为2L的密闭容器中,1mol A和1mo1 B进行反应:A(g)+3B(g) 2C(g) 经2分钟反应达到平衡,此时生成0.2mol C。
2C(g) 经2分钟反应达到平衡,此时生成0.2mol C。
下列说法正确的是
A.反应开始至2分钟时,以B浓度变化表示的反应速率为0.05mol/(L.min)
B.反应开始至2分钟时,A的转化率为5%
C.若其他条件不变,升高温度,A的体积分数增大,则该反应的△H<0
D.若其他条件不变,增大压强,化学反应速率的变化符合右侧示意图