实验室用下图装置制取少量溴苯,试填写下列空白。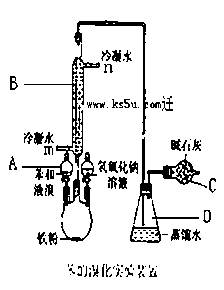
(1).写出仪器A的名称 ;B的名称 ;
(2).请你写出实验室制取溴苯的化学方程式 ___ ;
(3).长导管的下口为什么不插入锥形瓶的液面下
(4).反应完毕后向烧瓶A中滴加NaOH 溶液的作用是
(5).冷凝水的进水口是(填m或n) ,,图中干燥管C的作用是
实验室用下图装置制取少量溴苯,试填写下列空白。
(1).写出仪器A的名称 ;B的名称 ;
(2).请你写出实验室制取溴苯的化学方程式 ___ ;
(3).长导管的下口为什么不插入锥形瓶的液面下
(4).反应完毕后向烧瓶A中滴加NaOH 溶液的作用是
(5).冷凝水的进水口是(填m或n) ,,图中干燥管C的作用是