胃舒平主要成分是氢氧化铝,同时含有三硅酸镁(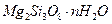 )等化合物。
)等化合物。
(1)三硅酸镁的氧化物形式为_______
(2)铝原子的原子结构示意图为 ,写出氢氧化铝与胃酸反应的离子方程式 。
(3)Al2O3、MgO和SiO2都可以制耐火材料, 其原因是______。
| A. Al2O3、MgO和SiO2都不溶于水 | B.Al2O3、MgO和SiO2都是白色固体 |
C.Al2O3、MgO和SiO 2都是氧化物 2都是氧化物  |
D.Al2O3、MgO和SiO2都有很高的熔点 |
胃舒平主要成分是氢氧化铝,同时含有三硅酸镁(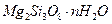 )等化合物。
)等化合物。
(1)三硅酸镁的氧化物形式为_______
(2)铝原子的原子结构示意图为 ,写出氢氧化铝与胃酸反应的离子方程式 。
(3)Al2O3、MgO和SiO2都可以制耐火材料, 其原因是______。
| A. Al2O3、MgO和SiO2都不溶于水 | B.Al2O3、MgO和SiO2都是白色固体 |
C.Al2O3、MgO和SiO 2都是氧化物 2都是氧化物  |
D.Al2O3、MgO和SiO2都有很高的熔点 |