利用芳香烃X和链烃Y可以合成紫外线吸收剂BAD,已知G不能发生银镜反应,BAD结构简式为:
OHCOOCCH3CH3OOCOH
BAD的合成路线如下: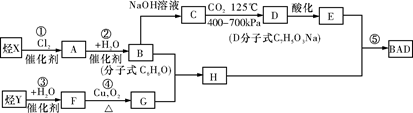
试回答下列问题:
(1)写出下列物质的结构简式:Y ;D ;
H 。
(2)属于取代反应的有 ①②⑤ (填数字序号)。
(3)1mol BAD最多可与含 mol NaOH的溶液完全反应。
(4)写出反应④的化学方程式 。
利用芳香烃X和链烃Y可以合成紫外线吸收剂BAD,已知G不能发生银镜反应,BAD结构简式为:
OHCOOCCH3CH3OOCOH
BAD的合成路线如下:
试回答下列问题:
(1)写出下列物质的结构简式:Y ;D ;
H 。
(2)属于取代反应的有 ①②⑤ (填数字序号)。
(3)1mol BAD最多可与含 mol NaOH的溶液完全反应。
(4)写出反应④的化学方程式 。