X(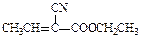 )是合成某种手术用粘合剂的单体,X的合成路线如下:
)是合成某种手术用粘合剂的单体,X的合成路线如下: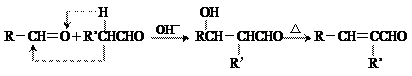
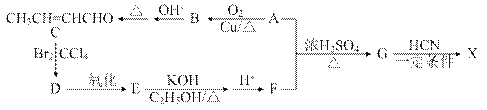
已知:
请回答下列问题:
⑴由单体X合成所得高分子粘合剂的结构简式是 ▲ 。
⑵物质C中所含官能团的名称是 ▲ 。
⑶写出由A→B的反应方程式: ▲ 。
⑷C→D、D→E的反应顺序能否颠倒并说明理由 ▲ 。
⑸C→D、A+F→G的反应类型依次为 ▲ 、 ▲ 反应。
⑹F的同分异构体中,属于酯类且含有“-C≡C-”结构,除了CH3COOC≡CH、 HCOOC≡CCH3外,还有的结构简式为 ▲ 、 ▲ 。
X(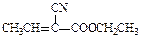 )是合成某种手术用粘合剂的单体,X的合成路线如下:
)是合成某种手术用粘合剂的单体,X的合成路线如下: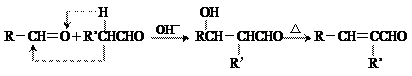

已知:
请回答下列问题:
⑴由单体X合成所得高分子粘合剂的结构简式是 ▲ 。
⑵物质C中所含官能团的名称是 ▲ 。
⑶写出由A→B的反应方程式: ▲ 。
⑷C→D、D→E的反应顺序能否颠倒并说明理由 ▲ 。
⑸C→D、A+F→G的反应类型依次为 ▲ 、 ▲ 反应。
⑹F的同分异构体中,属于酯类且含有“-C≡C-”结构,除了CH3COOC≡CH、 HCOOC≡CCH3外,还有的结构简式为 ▲ 、 ▲ 。