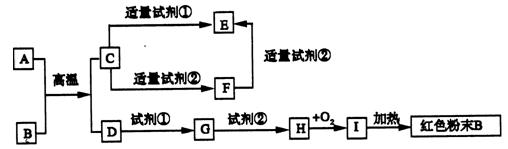
下图为中学化学中常见物质的转化关系,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物,试推断:
(1)写 出物质的化学式:
出物质的化学式:
(2)写出下列反应的方程式:
C →F的离子方程式:_____________________________________________
→F的离子方程式:_____________________________________________
H→I的化学方程式:______________________________________________
下图为中学化学中常见物质的转化关系,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物,试推断:

(1)写 出物质的化学式:
出物质的化学式:
(2)写出下列反应的方程式:
C →F的离子方程式:_____________________________________________
→F的离子方程式:_____________________________________________
H→I的化学方程式:______________________________________________