图表示各物质之间的转化关系。已知:A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液。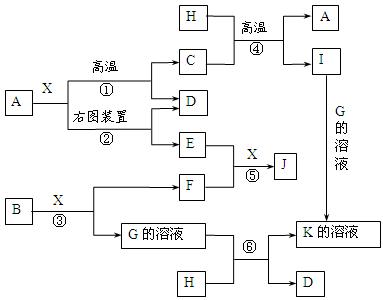
请 按要求填空:
按要求填空:
⑴写出B的化学式: 。
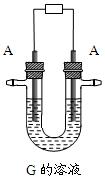
⑵写出用A作电极电解G溶液,在电极上生成E的反应式: ,反应⑤的现象是 。
⑶反应①的化学方程式是 ,
反应④在生产中有重要应用,被称为 反应。
⑷反应⑥的离子方程式是 。



 粤公网安备 44130202000953号
粤公网安备 44130202000953号