已知乳酸的结构简式为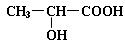 。试回答:
。试回答:
(1)乳酸分子中含有 和 两种官能团(写名称);
(2)乳酸与金属钠溶液反应的化学方程式为
(3)乳酸与Na2CO3溶液反应的化学方程式为
(4)当乳酸和浓硫酸共热时,能产生多种酯类化合物,任意写出两种该类产物的结构简式 、
已知乳酸的结构简式为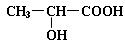 。试回答:
。试回答:
(1)乳酸分子中含有 和 两种官能团(写名称);
(2)乳酸与金属钠溶液反应的化学方程式为
(3)乳酸与Na2CO3溶液反应的化学方程式为
(4)当乳酸和浓硫酸共热时,能产生多种酯类化合物,任意写出两种该类产物的结构简式 、