(1)洗气瓶用途的延伸:利用如图所示的装置收集以下8种气体: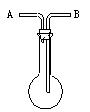
①H2、②Cl2、③CH4、④HCl、⑤NH3、⑥CO2、⑦O2、⑧SO2、⑨C2H4
(A)若烧瓶是干燥的,把装置颠倒放置由B口进气,可收集的气体有_______
(B)若在烧瓶内充满水,可收集的气体有________,气体应由____口进入
(2)下列实验能达到实验目的且符合安全要求的是 。
(1)洗气瓶用途的延伸:利用如图所示的装置收集以下8种气体:
①H2、②Cl2、③CH4、④HCl、⑤NH3、⑥CO2、⑦O2、⑧SO2、⑨C2H4
(A)若烧瓶是干燥的,把装置颠倒放置由B口进气,可收集的气体有_______
(B)若在烧瓶内充满水,可收集的气体有________,气体应由____口进入
(2)下列实验能达到实验目的且符合安全要求的是 。