甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。x、 A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,G的焰色反应为黄色。在一定条件下,各物质相互转化关系如下图:
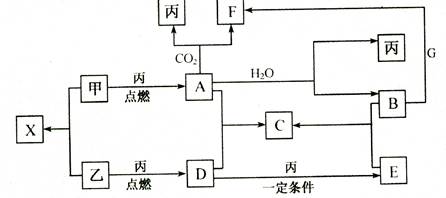
(1)用化学式表示:丙为 ,C为
(2)X的电子式为 。
(3)写出A与H2O反应的化学方程式:
(4)写出B与G溶液反应的离子方程式:
甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。x、 A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,G的焰色反应为黄色。在一定条件下,各物质相互转化关系如下图:

(1)用化学式表示:丙为 ,C为
(2)X的电子式为 。
(3)写出A与H2O反应的化学方程式:
(4)写出B与G溶液反应的离子方程式: