已知2H2O2=2H2O+O2↑。可以通过观察反应过程中O2的生成速度(即从气泡从溶液中释放的速度)来判断H2O2分解反应速度。请用所给的实验材料和用具设计实验,使其能验证过氧化氢酶的催化作用具有高效性。
实验材料与用具:适宜浓度的H2O2溶液, 3.5℅ FeCl3溶液,0.01℅过氧化氢酶溶液,恒温水浴锅,试管。
(1) 实验步骤:
①取2只试管,编号甲、乙。并向甲、乙两支试管中分别注入 的过氧化氢溶液,放入37℃恒温水浴锅中保温适当时间。
②向甲试管加入适量的3.5℅ FeCl3溶液,向乙试管加入 。
③观察各试管中 。
(2)实验结果预测及结论:
比较甲、乙试管O2的释放速度: 。
由此可得出的结论是:酶的催化作用具有 。
(3)如果仅将实验中的恒温水浴改为80℃,重复上述实验,O2的释放速度最快的是 。
原因是在此温度下,FeCl3催化作用加快,而过氧化氢酶因 。

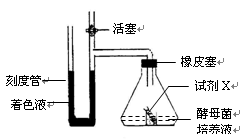

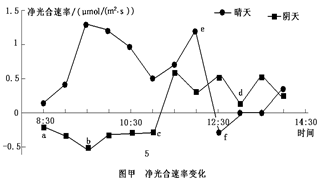

 ③假设红墨水滴每移动1 cm,植物体内的葡萄糖增加或减少1 g。那么该植物的细胞呼吸速率(分解葡萄糖速率)是g/h。白天光照15小时,一昼夜葡萄糖的积累量是g。(不考虑昼夜温差影响)
③假设红墨水滴每移动1 cm,植物体内的葡萄糖增加或减少1 g。那么该植物的细胞呼吸速率(分解葡萄糖速率)是g/h。白天光照15小时,一昼夜葡萄糖的积累量是g。(不考虑昼夜温差影响)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号