(1)把镁条投入盛有盐酸的敞口容器中,产生氢气速率变化如图所示。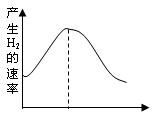
在反应过程中导致速率变化的因素有
①H+的浓度②镁条的表面积③溶液的温度④Cl—的浓度
(2)影响速率的有关因素有:物质本身的性质、浓度、温度、催化剂等方面,依据影响速率的有关因素分析下列问题:
①Mg和Fe均可以与O2反应, Mg在空气中可以点燃, Fe在空气中不能点燃,是由于 的影响;
②Fe在空气中加热不能燃烧,但在纯氧中可以,是由于 的影响;
(1)把镁条投入盛有盐酸的敞口容器中,产生氢气速率变化如图所示。
在反应过程中导致速率变化的因素有
①H+的浓度②镁条的表面积③溶液的温度④Cl—的浓度
(2)影响速率的有关因素有:物质本身的性质、浓度、温度、催化剂等方面,依据影响速率的有关因素分析下列问题:
①Mg和Fe均可以与O2反应, Mg在空气中可以点燃, Fe在空气中不能点燃,是由于 的影响;
②Fe在空气中加热不能燃烧,但在纯氧中可以,是由于 的影响;