工业上由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。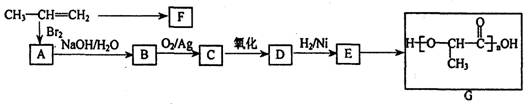
(1)聚合物F的结构简式是 。
(2)C与新制的Cu(OH)2共热转化为D的化学方程式是: 。
(3)D转化为E的化学方程式是 。
(4)在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简式是 。
工业上由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。
(1)聚合物F的结构简式是 。
(2)C与新制的Cu(OH)2共热转化为D的化学方程式是: 。
(3)D转化为E的化学方程式是 。
(4)在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简式是 。