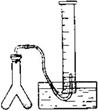
在室温和大气压强下,用图示的装置进行实验,测得 含90%的样品与水完全反应产生的气体体积。现欲在相同条件下,测定某电石试样中的质量分数,请回答下列问题:
(1)和水反应的化学方程式是。
(2)若反应刚结束时,观察到的实验现象如图所示,这时不能立即取出导气管,理由是。
(3)本实验中测量气体体积时应注意的事项有。
(4)如果电石试样质量为,测得气体体积为,则电石试样中的质量分数计算式()=。(杂质所生成的气体体积忽略不计)。
在室温和大气压强下,用图示的装置进行实验,测得 含90%的样品与水完全反应产生的气体体积。现欲在相同条件下,测定某电石试样中的质量分数,请回答下列问题:

(1)和水反应的化学方程式是。
(2)若反应刚结束时,观察到的实验现象如图所示,这时不能立即取出导气管,理由是。
(3)本实验中测量气体体积时应注意的事项有。
(4)如果电石试样质量为,测得气体体积为,则电石试样中的质量分数计算式()=。(杂质所生成的气体体积忽略不计)。