A是乙烯与水加成后的产物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。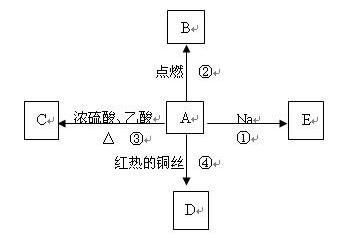
(1)A的结构简式为 ,它的官能团名称为 。
(2)若A中的氧原子为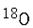
 ,则 A与乙酸的反应产物中含有
,则 A与乙酸的反应产物中含有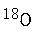 的物质是 (填化学式)。
的物质是 (填化学式)。
(3)写出下列反应的化学方程式
反应①
反应③ 
反应④
A是乙烯与水加成后的产物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。
(1)A的结构简式为 ,它的官能团名称为 。
(2)若A中的氧原子为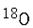
 ,则 A与乙酸的反应产物中含有
,则 A与乙酸的反应产物中含有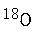 的物质是 (填化学式)。
的物质是 (填化学式)。
(3)写出下列反应的化学方程式
反应①
反应③ 
反应④