2011年6月,云南曲靖陆良化工实业有限公司5000多吨工业废料铬渣非法倾倒导致当地严重污染。+6价铬易被人体吸收,可致癌;+3价铬不易被人体吸收,毒性小。工业含铬废水的处理方法之一是将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的NaCl后进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(已知:常温下Ksp Fe(OH)3=2.6×10-39,Ksp Cr(OH)3=6.0×10-31)
(1)若阳极铁质量减少16.8g,则理论上被还原的Cr2O72-的物质的量为mol。
(2)已知电解后的溶液中c(Fe3+)为2.6×10-13 mol·L-1,则溶液中Cr3+浓度为mol·L-1。
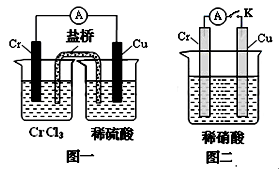
(3)在下图装置中,观察到图一装置铜电极上产生大量的无色气泡,而在图二装置中当开关K断开时,铬电极无现象,K闭合时,铬电极上产生大量无色气体,并变成红棕色气体。根据上述现象试推测金属铬的两个重要化学性质、 。
 O3和NaOH的混合物共ag,将容器加热至200℃,经充分反应后,排除其中的气体,冷却,称得剩余固体质量为bg,求容器中(NH4)2CO3和NaOH各多少克?
O3和NaOH的混合物共ag,将容器加热至200℃,经充分反应后,排除其中的气体,冷却,称得剩余固体质量为bg,求容器中(NH4)2CO3和NaOH各多少克? O3和NaOH的混合物共ag,将容器加热至200℃,经充分反应后,排除其中的气体,冷却,称得剩余固体质量为bg,求容器中(NH4)2CO3和NaOH各多少克?
O3和NaOH的混合物共ag,将容器加热至200℃,经充分反应后,排除其中的气体,冷却,称得剩余固体质量为bg,求容器中(NH4)2CO3和NaOH各多少克?