(1)下图分别是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是 。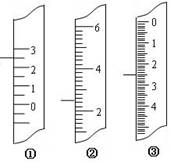
A.①是量筒,读数为2.5mL
B.②是量筒,读数为2.5mL



 C.③是滴定管,读数为3.5mL
C.③是滴定管,读数为3.5mL
D.①是温度计,读数为2.5℃
(2)实验室里不同化学试剂的保存方法不尽相同。下图中A、B、C、D、E是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下面的括号内(多选倒扣分):
①NaOH溶液 ②浓硫酸 ③Na2CO3溶液 ④白磷 ⑤大理石 ⑥酒精 ⑦氯水 ⑧浓硝酸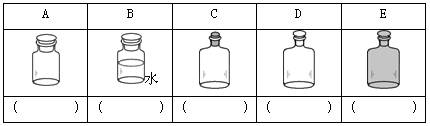
(1)下图分别是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是 。
A.①是量筒,读数为2.5mL
B.②是量筒,读数为2.5mL



 C.③是滴定管,读数为3.5mL
C.③是滴定管,读数为3.5mL
D.①是温度计,读数为2.5℃
(2)实验室里不同化学试剂的保存方法不尽相同。下图中A、B、C、D、E是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下面的括号内(多选倒扣分):
①NaOH溶液 ②浓硫酸 ③Na2CO3溶液 ④白磷 ⑤大理石 ⑥酒精 ⑦氯水 ⑧浓硝酸