(16分)聚苯乙烯的结构为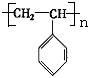 ,试回答下列问题:
,试回答下列问题:
(1)聚苯乙烯的链节是_________________,单体是___________________;
(2)实验测得聚苯乙烯的相对分子质量(平均值)为52000,则该高聚物的聚合度n为_________。
(3)已知聚苯乙烯为线性结构的高分子化合物,试推测:_________(“能”与“不能”)溶于CHCl3,具有__________(填“热塑”或“热固”)性。
(16分)聚苯乙烯的结构为 ,试回答下列问题:
,试回答下列问题:
(1)聚苯乙烯的链节是_________________,单体是___________________;
(2)实验测得聚苯乙烯的相对分子质量(平均值)为52000,则该高聚物的聚合度n为_________。
(3)已知聚苯乙烯为线性结构的高分子化合物,试推测:_________(“能”与“不能”)溶于CHCl3,具有__________(填“热塑”或“热固”)性。