某晶体的粒子结构如图5—10所示:正六面体的8个顶点上为A粒子,12个棱的中点上为B粒子,6个面的中心上为C粒子,六面体的中心上为D粒子。那么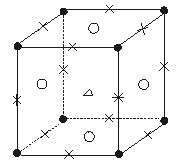
图5—10
该晶体中A、B、C、D 4种粒子的个数比为( )
A.1∶3∶3∶1 B.3∶1∶3∶1
C.1∶1∶3∶3 D.1∶3∶1∶3
某晶体的粒子结构如图5—10所示:正六面体的8个顶点上为A粒子,12个棱的中点上为B粒子,6个面的中心上为C粒子,六面体的中心上为D粒子。那么
图5—10
该晶体中A、B、C、D 4种粒子的个数比为( )
A.1∶3∶3∶1 B.3∶1∶3∶1
C.1∶1∶3∶3 D.1∶3∶1∶3