|
实验室制取气体常用的装置如下列图示,请回答下列问题:(选用装置时填字母编号)

(1)若实验室选用装置C制取氨气,则反应的化学方程式为
________________________________________
 ______________________,
______________________,检验NH3收
 满的方法:____________________________________________________;
满的方法:____________________________________________________;(2)若实验室利用过氧化钠与水反应制取氧气,则应选择__________装置,有关反应的化学方程式为:________________________________________________。



 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0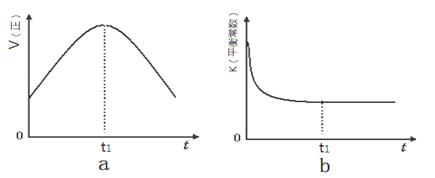
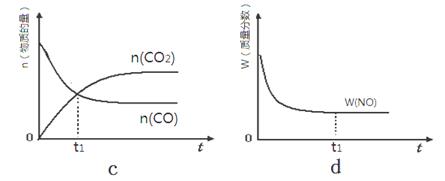
 N2O4(g)△H=-56.9 kJ/mol
N2O4(g)△H=-56.9 kJ/mol
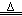 CO+CO2+(x+1)H2O。下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题。
CO+CO2+(x+1)H2O。下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题。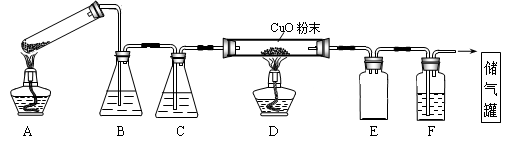
 [Fe(H2O)6-n(OH)n]3-n(黄色) + nH3O+(n = 0~6) ;
[Fe(H2O)6-n(OH)n]3-n(黄色) + nH3O+(n = 0~6) ;


 [Fe(H2O)6]3+ + 4Cl-,得出此结论的理由是 。
[Fe(H2O)6]3+ + 4Cl-,得出此结论的理由是 。 粤公网安备 44130202000953号
粤公网安备 44130202000953号