将1 mol H2(g)和2 mol I2 (g)置于某2L密闭容器中,在一定温度下发生反应:H2(g)+I2(g) 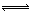 2HI(g);ΔH<0 ,并达到平衡。HI的体积分数ω(HI)随时间变化如图(Ⅰ)所示,若改变反应条件,ω(HI)的变化曲线如图(Ⅱ)所示,则改变的条件可能是 ( )
2HI(g);ΔH<0 ,并达到平衡。HI的体积分数ω(HI)随时间变化如图(Ⅰ)所示,若改变反应条件,ω(HI)的变化曲线如图(Ⅱ)所示,则改变的条件可能是 ( ) 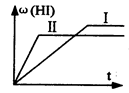
| A.恒温条件下,加入适当催化剂 | B.恒温,恒容下,充入氦气 |
| C.恒容条件下升高温度 | D.恒温,恒压下,充入氦气 |
将1 mol H2(g)和2 mol I2 (g)置于某2L密闭容器中,在一定温度下发生反应:H2(g)+I2(g) 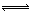 2HI(g);ΔH<0 ,并达到平衡。HI的体积分数ω(HI)随时间变化如图(Ⅰ)所示,若改变反应条件,ω(HI)的变化曲线如图(Ⅱ)所示,则改变的条件可能是 ( )
2HI(g);ΔH<0 ,并达到平衡。HI的体积分数ω(HI)随时间变化如图(Ⅰ)所示,若改变反应条件,ω(HI)的变化曲线如图(Ⅱ)所示,则改变的条件可能是 ( ) 
| A.恒温条件下,加入适当催化剂 | B.恒温,恒容下,充入氦气 |
| C.恒容条件下升高温度 | D.恒温,恒压下,充入氦气 |