现有下列各化合物: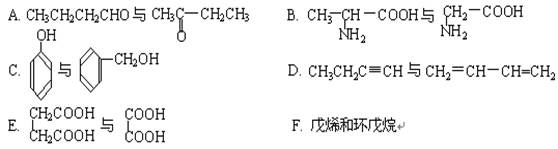
①上述各组化合物属于同系物的是 ,属于同分异构体的是 (填入编号)。
②上述化合物中的含氧官能团是(写名称) ;
根据官能团的特点可将C中两化合物划分为 类和 类。
③若将A中两化合物看作是某单烯烃被酸性高锰酸钾溶液氧化生成的,则该单烯烃的结构简式为 。
现有下列各化合物:
①上述各组化合物属于同系物的是 ,属于同分异构体的是 (填入编号)。
②上述化合物中的含氧官能团是(写名称) ;
根据官能团的特点可将C中两化合物划分为 类和 类。
③若将A中两化合物看作是某单烯烃被酸性高锰酸钾溶液氧化生成的,则该单烯烃的结构简式为 。