在密闭容器中有反应:aX(g)+bY(g) nW(g);ΔH=Q,某同学根据此反应在不同条件下的实验数据,作出如下曲线: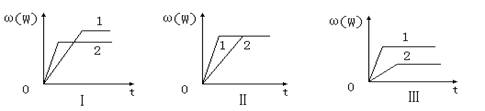
其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是
| A.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b>n |
| B.图Ⅱ可能是同温同压催化剂对反应的影响,且1的催化剂效果更好 |
| C.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b |
| D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0 |
在密闭容器中有反应:aX(g)+bY(g) nW(g);ΔH=Q,某同学根据此反应在不同条件下的实验数据,作出如下曲线:
其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是
| A.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b>n |
| B.图Ⅱ可能是同温同压催化剂对反应的影响,且1的催化剂效果更好 |
| C.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b |
| D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0 |