(16分)现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型。A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态。请回答下列问题(填空时用实际符号):
(1)C的元素符号是 ;元素F在周期表中的位置 。
(2)B与D一般情况下可形成两种常见气态化合物,假若现在科学家制出另一种直线型气态化合物 B2D2分子,且各原子最外层都满足8电子结构,则B2D2电子式为 ,其固体时的晶体类型是 。
(3)最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4分子。C4分子结构如右图所示,已知断裂lmolC-C吸收167kJ热量,生成Imo1C=C放出942kJ热量。根据以上信息和数据,下列说法正确的是 。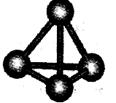
① C4属于一种新型的化合物
② C4沸点比P4(白磷)低
③ lmol C4气体转变为C2吸收882kJ热量
④ C4与C2互为同素异形体
⑤ C4稳定性比P4(白磷)差
⑥ C4属于原子晶体
⑦ C4和P4 (白磷)的晶体都属于分子晶体
⑧ C4与C2互为同分异构体
(4)C与F两种元素形成一种化合物分子,各原子最外层达8电子结构,则该分子的结构式为 ,其空间构型为 。
(5)为了除去化合物乙(A2ED4);)稀溶液中混有的A2ED3,常采用A2D2为氧化剂,发生反应的离子方程式为:
(6)E与F形成的化合物E2F2在橡胶工业上有重要用途,遇水易水解,其空间结构与A2D2极为相似。对此以下说法正确的是 。
a.E2F2的结构式为:F- E—E- F
b.E2F2为含有极性键和非极性键的非极性分子
c.E2Br2与E2F2结构相似,熔沸点:E2Br2> E2F2
d.E2F2与H2O反应的化学方程式可能为:2 E2F2+2H2O=EO2↑+ 3E↓+4HF
(7)举出一种事实说明E与F的非金属性强弱(用化学方程式或用语言文字表达均可):
 粤公网安备 44130202000953号
粤公网安备 44130202000953号