工业上为了使原料和能量得到充分的利用,常常采用循环操作。
Ⅰ、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
MnFe2O4的制备:
| |
开始沉淀 |
完全沉淀 |
| Fe3+ |
2.7 |
3.7 |
| Mn2+ |
8.3 |
10.4 |
已知Fe3+、Mn2+沉淀的pH如右表所示。
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质
的量之比应为 __________。
(2)控制pH的操作中m的值为 。
Ⅱ、用MnFe2O4热化学循环制取氢气:

(3)由上可知,表示H2燃烧热的热化学方程式是__________________________ 。
(4)该热化学循环制取氢气的优点是_______________(填字母编号)。
A.过程简单、无污染
B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl在一定条件下通过下图的循环流程制取太阳能材料高纯硅。
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是___________________。
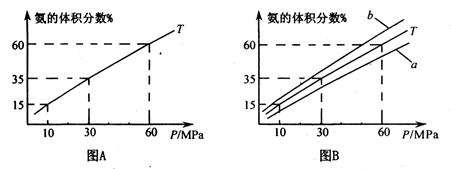
 所需的氢气可由甲烷与水反应制得,反应的热化学方程式为:
所需的氢气可由甲烷与水反应制得,反应的热化学方程式为: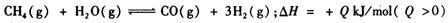
 物质的物质的量变化如下表
物质的物质的量变化如下表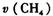 =______。
=______。 2
2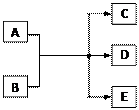

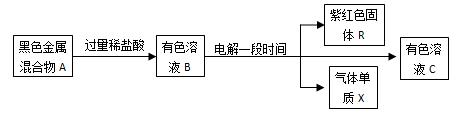
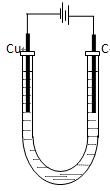
 反应产物已略去)。
反应产物已略去)。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号