在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3Sn2+ + 18Cl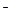 + aH3AsO3 + bH+=aAs + 3SnCl6
+ aH3AsO3 + bH+=aAs + 3SnCl6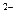 + cM,关于该反应的说法中正确的组合是
+ cM,关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3; ② 还原性:Cl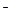 >As; ③ 每生成0.1 mol As,还原剂失去的电子为0.3mol; ④ M为OH
>As; ③ 每生成0.1 mol As,还原剂失去的电子为0.3mol; ④ M为OH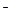 ; ⑤ a=2,b=6
; ⑤ a=2,b=6
| A.只有①③ | B.①③⑤ | C.①②③④ | D.①②④⑤ |
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3Sn2+ + 18Cl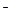 + aH3AsO3 + bH+=aAs + 3SnCl6
+ aH3AsO3 + bH+=aAs + 3SnCl6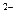 + cM,关于该反应的说法中正确的组合是
+ cM,关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3; ② 还原性:Cl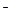 >As; ③ 每生成0.1 mol As,还原剂失去的电子为0.3mol; ④ M为OH
>As; ③ 每生成0.1 mol As,还原剂失去的电子为0.3mol; ④ M为OH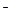 ; ⑤ a=2,b=6
; ⑤ a=2,b=6
| A.只有①③ | B.①③⑤ | C.①②③④ | D.①②④⑤ |