为测定一种气态烃A的分子式,取一定量的A置于密闭容器中燃烧,定性实验表明产物是CO2、CO、水蒸气。学生甲、乙设计了如下两个方案,均认为根据自己的方案能求出A的实验式。他们测得的有关数据如下(图中的箭头表示气体的流向,实验前系统内的空气已排除)。试完成下列问题:
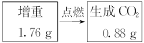


(1)两种方案能否都可求出A的实验式(即C、H原子数比)?
(2)若能求,通过计算求出A的实验式。
(3)若要确定A的分子式,是否还需要测定其他数据?如果需要,该测定哪些数据?
为测定一种气态烃A的分子式,取一定量的A置于密闭容器中燃烧,定性实验表明产物是CO2、CO、水蒸气。学生甲、乙设计了如下两个方案,均认为根据自己的方案能求出A的实验式。他们测得的有关数据如下(图中的箭头表示气体的流向,实验前系统内的空气已排除)。试完成下列问题:



(1)两种方案能否都可求出A的实验式(即C、H原子数比)?
(2)若能求,通过计算求出A的实验式。
(3)若要确定A的分子式,是否还需要测定其他数据?如果需要,该测定哪些数据?