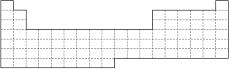
(1)在上面元素周期表中画出金属元素与非金属元素的分界线。
(2)根据NaH的存在,有人提议可把氢元素放在ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的________族。
(3)第四周期有A、B、C、D四种元素,其最外层电子数依次为1、2、2、7,其原子序数按A、B、C、D的顺序增大,又已知A、B的次外层电子数为8,C、D的次外层电子数为18。请将A、B、C、D用元素符号填写在上面周期表中的对应位置上。

(1)在上面元素周期表中画出金属元素与非金属元素的分界线。
(2)根据NaH的存在,有人提议可把氢元素放在ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的________族。
(3)第四周期有A、B、C、D四种元素,其最外层电子数依次为1、2、2、7,其原子序数按A、B、C、D的顺序增大,又已知A、B的次外层电子数为8,C、D的次外层电子数为18。请将A、B、C、D用元素符号填写在上面周期表中的对应位置上。