(11分) 芳香族羧酸通常用芳香烃的氧化来制备。芳香烃的苯环比较稳定,难以氧化,而环上的支链不论长短,在强烈氧化时,最终能氧化成羧基。某同学用甲苯的氧化反应制备苯甲酸。
反应原理:

反应试剂、产物的物理常数:
名称
|
相对分
子质量
|
性状
|
熔点
|
沸点
|
密度
|
溶解度
|
水
|
乙醇
|
乙醚
|
甲苯
|
92
|
无色液体易燃易挥发
|
-95
|
110.6
|
0.8669
|
不溶
|
易溶
|
易溶
|
苯甲酸
|
122
|
白色片状或针状晶体
|
122.4
|
248
|
1.2659
|
微溶
|
易溶
|
易溶
|
主要实验装置和流程如下:
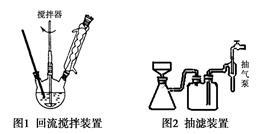
实验方法:一定量的甲苯和KMnO4溶液置于图1装置中,在90℃时, 反应一段时间,再停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。

(1)操作Ⅰ所需的玻璃仪器为________________;操作Ⅱ为______________。
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,加亚硫酸氢钾的目的是__________________________。
(3)下列关于仪器的组装或者使用正确的是________。
A.抽滤可以加快过滤速度,得到较干燥的沉淀
B.安装电动搅拌器时,搅拌器下端不能与三颈烧瓶底、温度计等接触
C.图1回流搅拌装置应采用直接加热的方法
D.冷凝管中水的流向是下进上出
(4)除去残留在苯甲酸中的甲苯应先加入_________,分液,水层再加入 ,然后抽滤,干燥即可得到苯甲酸。
(5)纯度测定:称取1.220 g产品,配成100 mL溶液,取其中25.00 mL溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为______________。