I.实验室要用98%(ρ=1.84g·cm-3)的硫酸配制3.68mol·L-1的硫酸溶液500mL
(1)需准确量取98%的硫酸mL。
(2)准确量取一定体积的98%的硫酸后,要配制3.68mol·L-1的硫酸溶液500mL,必须用到的实验仪器是(填写序号):.
①500mL量筒②烧杯③1000mL容量瓶④500mL容量瓶⑤天平⑥胶头滴管⑦锥形瓶⑧玻璃棒⑨酸式滴定管
(3)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是。
| A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒。 |
| B.烧杯内的稀硫酸未冷却至室温就转移至容量瓶中 |
| C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切。 |
| D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切。 |
II. 某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:
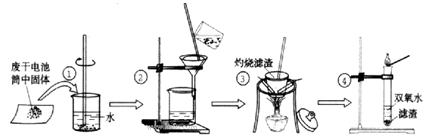
普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
⑴.操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为(填化学式);
(2)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:(答案写在答题卷上)
实验目的
|
操作
|
实验现象
|
结论
|
1.检验Cl—
|
取少许滤液于试管中,加入
|
产生白色沉淀
|
含有Cl—
|
2.检验NH4+
|
取少许滤液于试管中,加入
|

|
含有NH4+
|
3.检验Zn2+
|
取少许滤液于试管中,加入稀氨水
|
先产生白色沉淀,继续加入氨水,沉淀又溶解
|
含有Zn2+
|