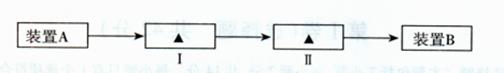
(8分)有甲、乙两位同学想利用下列装置及化学试剂,对实验室制取并收集氨气的实验进行改进。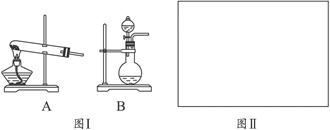
化学试剂:①NH4Cl固体 ②浓氨水 ③固体NaOH
(1)甲同学想方便快速制取少量氨气,应选择的装置是_________ (填序号)。
选用试剂是_________(填序号),选用上述试剂制氨气的理由是__________________。
(2)乙同学建议,把教材中实验室制取氨气的收集装置由大试管改为集气瓶且瓶口向上收集氨气,并确保不污染环境,请你根据其设想完成问题:
若用排气法收集氨气,请在图Ⅱ的方框内画出其气体收集装置和尾气吸收装置,标出所用试剂(自选)名称。
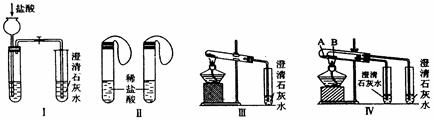
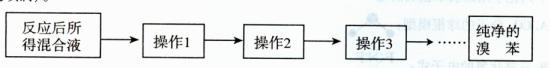
 。操作2目的:。
。操作2目的:。 8分)亚铁盐在空气中易被氧化,但形成复盐可稳定存在。硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O]是一种重要化学试剂,实验室可用纯铁片来制
8分)亚铁盐在空气中易被氧化,但形成复盐可稳定存在。硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O]是一种重要化学试剂,实验室可用纯铁片来制 取硫酸亚铁铵,流程如下:
取硫酸亚铁铵,流程如下: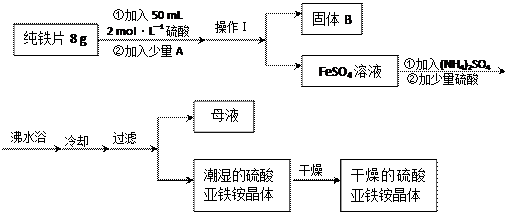
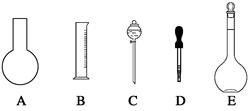
 ,所用主要仪器和用品有(铁架台、铁圈除外)
,所用主要仪器和用品有(铁架台、铁圈除外)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号